Február végétől elérhetővé válhat az öt év alatti gyermekek számára szánt védőoltás Amerikában
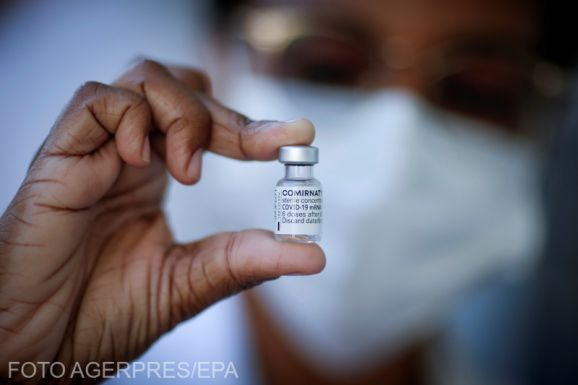
A Pfizer öt év alatti gyermekek számára kifejlesztett, koronavírus elleni oltása február végén elérhetővé válhat Amerikában. A cég a következő hetekben kaphatja meg a jóváhagyást – írja a The Washington Post.
A Pfizer és német partnere, a BionNTech kedden nyújtja be a hathónapos és ötéves közötti gyermekek számára szánt vakcina gyorsított engedélyezési kérelmét az Amerikai Egyesült Államok Szövetségi Élelmiszer- és Gyógyszerfelügyeleti Hatóságához (FDA), az FDA ugyanis felszólította a két partnercéget, hogy nyújtsanak be engedélykérelmet ahhoz, hogy a hatóságok felmérhessék a kétdózisú vakcina hatását.
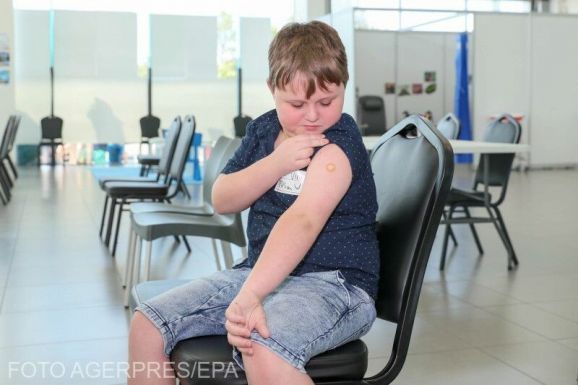
Ez lenne az első oltás, amelyet a fent említett korcsoport is megkaphat. Az idősebb gyerekek oltása már engedélyezett, február 26-án már Romániában is megkezdődött az 5–11 éves korosztály oltása.
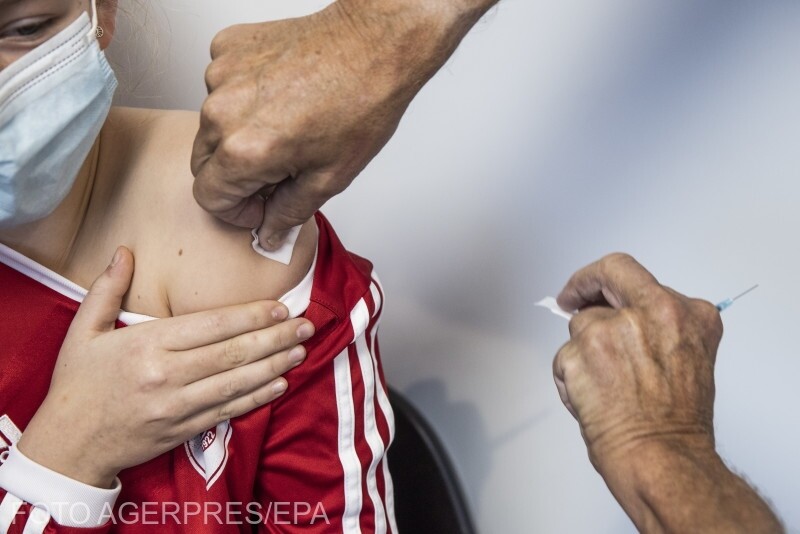
A vállalatok az elmúlt hónapokban egy harmadik adagot is teszteltek, miután a két injekció beadásának eredményei nem bizonyultak meggyőzőnek. Az eredmények szerint az oltás biztonságos, de két adag nem biztosít elég erős immunizálást minden korcsoport számára. Egyelőre nem állnak rendelkezésre információk a harmadik dózisról, tehát március vége előtt a hatóságok nem engedélyeznék a gyermekeknek szánt oltás harmadik adagját.
Az amerikai kormány sürgetné az oltás engedélyeztetését. Múlt pénteken a Pfizer új adatokat mutatott be az egészségügyi tisztviselőknek a kisgyermekeknek szánt oltásról. Az FDA külső tanácsadói várhatóan február közepén ülnek össze, hogy tárgyaljanak a bevezetendő kétadagos vakcináról. Decemberben a Pfizer és BioNTech kijelentette, hogy az oltás a 2–4 éveseknél nem váltott ki – a serdülők és felnőttek körében már tapasztalt – megfelelő immunitást. A két dózis azonban jó immunválaszt adott a hathónapos és kétéves közöttiek csoportjában.
CSAK SAJÁT


.jpg)



.jpg)



.jpg)
.png)
.jpg)


.jpg)


