EMA: kivizsgálják a Janssen-vakcinával összefüggésbe hozott vérrögképződéses eseteket
Az Európai Gyógyszerügynökség (EMA) megkezdte a Johnson and Johnson gyógyszeripari vállalata, a Janssen által az új típusú koronavírus ellen kifejlesztett oltóanyaggal végzett oltásokat követően jelentett nagyon ritka vérrögképződéses estek kivizsgálását – közölte az uniós gyógyszerügynökség pénteken.
Az Európai Unió gyógyszerfelügyeleti hatóságának szerepét betöltő amszterdami székhelyű ügynökség közleményében kiemelte: mostanáig mindössze négy alkalommal jelentettek tromboembóliás eseményeket, azaz érelzáródás veszélyével járó vérrögképződést azoknál, akiket a Janssen vakcinájával beoltottak.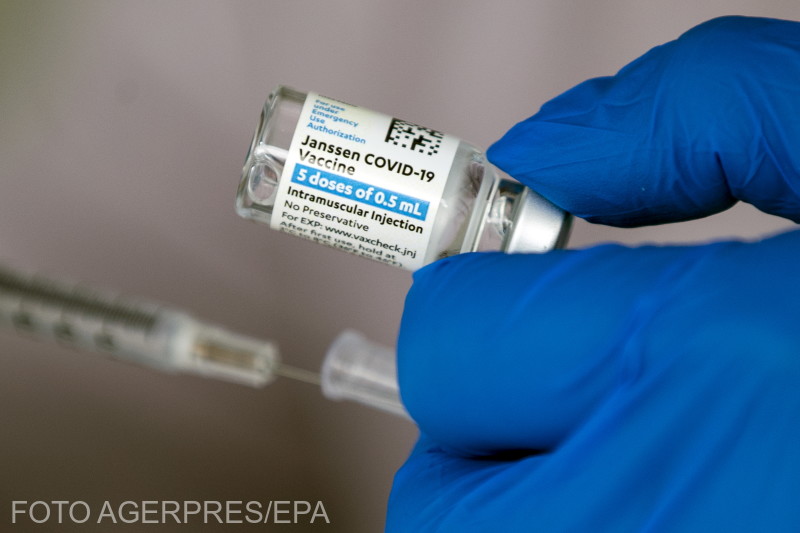
Elmondták, hogy a négy szokatlan véralvadással járó esetből egy a klinikai vizsgálat szakaszában meg nem nevezett helyszínen, három pedig a vakcina beadását követően fordult elő az Egyesült Államokban. Az egyik eset halálos kimenetelű volt – tették hozzá. Kiemelték: kivizsgálásra vár, hogy van-e okozati összefüggés a Janssen oltóanyaga és a kisszámú vérrögképződéses eset között. Az ügynökség illetékes kockázatértékelő bizottsága (PRAC) megkezdte az esetek felülvizsgálatát annak megállapítására, hogy szükség-e a vakcina termékinformációjának frissítése.
A Janssen koronavírus elleni oltóanyagát jelenleg csak az Egyesült Államokban alkalmazzák, a vakcina március 11-én kapott ideiglenes forgalomba hozatali engedélyt az Európai Unióban. Az oltóanyag bevezetése még egyetlen EU-tagállamban sem kezdődött el, alkalmazása Európában a következő hetekben várható. Az Európai Bizottság október 8-án kötött megállapodást a Johnson & Johnson vállalattal 200 millió adag oltóanyag beszerzéséről, további 200 millió dózis vásárlásának lehetőségével.
CSAK SAJÁT
A Janssen által kifejlesztett oltóanyag arra a technológiai platformra támaszkodik, amelyet már használtak a gyógyszergyár ebola elleni oltóanyagának, valamint a Zika-, az RSV- és a HIV-vírus elleni vakcinák kifejlesztéséhez és gyártásához. Az oltóanyagban ártalmatlanított adenovírussal juttatják be a koronavírusra jellemző tüskefehérjét a szervezetbe. Az immunrendszer ezt követően idegen anyagként kezeli ezt a fehérjét, és természetes védekezésként antitesteket és a fehérvérsejtek csoportjához tartozó T-sejteket termel ellene. A vakcinában található adenovírus nem képes szaporodni, és nem okoz betegséget.
During its April meeting, EMA’s safety committee, the #PRAC, carried out its broad range of responsibilities, which cover all aspects of the risk management of the use of medicines, including #COVID19vaccines. Read more:
— EU Medicines Agency (@EMA_News) April 9, 2021
https://t.co/BSurWDTBs4 pic.twitter.com/zFau6OmBuL
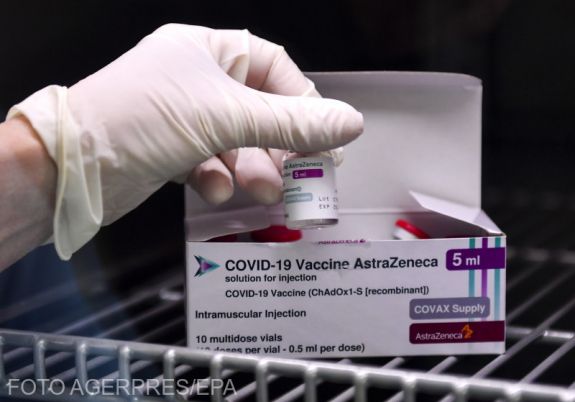
Az Európai Gyógyszerügynökség szerdán tette közzé az AstraZeneca brit-svéd gyógyszergyártó és az Oxfordi Egyetem Vaxzevria névre keresztelt oltóanyagával kapcsolatban felvetődött vérrögképződéses esetek kivizsgálásának részeredményét. Az ügynökség arra a következtetésre jutott, hogy lehetséges az összefüggés a vérrögképződéssel összefüggő rendellenességek korábban jelzett nagyon ritka esetei és az AstraZeneca gyógyszergyár koronavírus elleni oltóanyaga között, a vakcina előnyei azonban továbbra is felülmúlják a lehetséges mellékhatások kockázatait. Mint közölték: a vérrögképződés esetleges veszélyét fel kell tüntetni a vakcina „nagyon ritka mellékhatásaként".
Kapcsolódó
Az értékelés alátámasztja, hogy az AstraZeneca vakcinája biztonságos, és hatékonyan képes megelőzni a koronavírus okozta betegséget, csökkenti a kórházi kezelés és halálesetek kockázatát – tették hozzá. Hangsúlyozták továbbá, hogy a koronavírus okozta elhalálozás kockázata sokkal magasabb, mint a vérrögképződés esetleges, nagyon ritka előfordulása. Az ügynökség nem javasolt semmiféle korlátozást az oltóanyag alkalmazása tekintetében a 18 éveseknél idősebbek esetében. A vakcina további vizsgálata folytatódik – közölték.

.jpg)










_(1).jpg)



